
一、概述
ㅤㅤ新兽药注册是我国兽医药品管理的重要环节,旨在保障动物健康、人类食品安全以及生态环境的和谐稳定。随着我国畜牧业和养殖业的快速发展,兽药市场需求逐年攀升,兽药种类和数量不断丰富,兽药的研究与开发成为推动行业进步的关键因素。然而,兽药的研发和注册过程中存在诸多挑战,如研发投入不足、注册审批周期长、技术要求高等问题。为了进一步提高兽药注册的效率和质量,我国政府及相关部门不断加大对兽药注册管理的改革力度,完善法规政策,加强技术创新,推动兽药产业健康发展。在此背景下,兽药注册显得尤为重要,不仅关乎动物疾病的防控,更影响到我国畜牧业的可持续发展。
二、谁是新兽药注册主体?
ㅤㅤ兽药生产企业或向中国出口的境外企业,境外企业必须由出口方驻中国境内的办事机构或由其委托的中国境内代理机构向农业部提出申请。
ㅤㅤ联合研制的新兽药,可以由其中一个单位申请注册或联合申请注册,但不得重复申请注册;联合申请注册的,应当共同署名作为该新兽药的申请人。
三、新兽药注册申请条件是什么?
ㅤㅤ1. 新兽药注册申请人应当在完成临床试验后,向农业农村部提出申请,并按《兽药注册资料要求》提交相关资料。
ㅤㅤ2. 联合研制的新兽药,可以由其中一个单位申请注册或联合申请注册,但不得重复申请注册;联合申请注册的,应当共同署名作为该新兽药的申请人。申请新兽药注册所报送的资料应当完整、规范,数据必须真实、可靠。
ㅤㅤ3. 申请新兽药注册时,申请人应当提交保证书,承诺对他人的知识产权不构成侵权并对可能的侵权后果负责,保证自行取得的试验数据的真实性。
ㅤㅤ4. 申报资料含有境外兽药试验研究资料的,应当附具境外研究机构提供的资料项目、页码情况说明和该机构经公证的合法登记证明文件。
四、有哪些禁止性要求?
ㅤㅤ1. 与尚处于监测期内的新兽药相同的产品,申请人不能证明数据为自己取得的兽药不予受理。
ㅤㅤ2. 经基因工程技术获得,未通过生物安全评价的灭活疫苗、诊断制品之外的兽药不予受理。
五、新兽药注册需要准备哪些材料?
ㅤㅤ1. 《兽药注册申请表》一式二份(原件)。
ㅤㅤ2. 申请人合法登记证明文件,包括营业执照、法人证书等(复印件)。
ㅤㅤ3. 属于转基因生物技术产品的(灭活疫苗和诊断制品除外),需提供农业转基因生物安全证书(复印件)。
ㅤㅤ4. 连续三批样品及其批生产检验记录、检验报告单。
ㅤㅤ5. 属于生物制品的,还应当提供菌(毒、虫)种、细胞等有关材料。
ㅤㅤ6. 根据新兽药不同类别,按照《兽药注册资料要求》等有关规定提交其他注册资料。
ㅤㅤ7. 注册资料一式两份,A4纸双面复印装订成册,加盖所有注册申请单位公章(与注册申请表申报单位一致)。申报资料内容齐全,应有目录、连续页码,所有委托试验提供试验报告原件,并附试验结果原始图谱和照片等。
ㅤㅤ8. 上述申请材料中以下证明材料可选择采用书面承诺方式,以告知承诺书(见附件)替代。营业执照、法人证书复印件。
六、新兽药注册流程
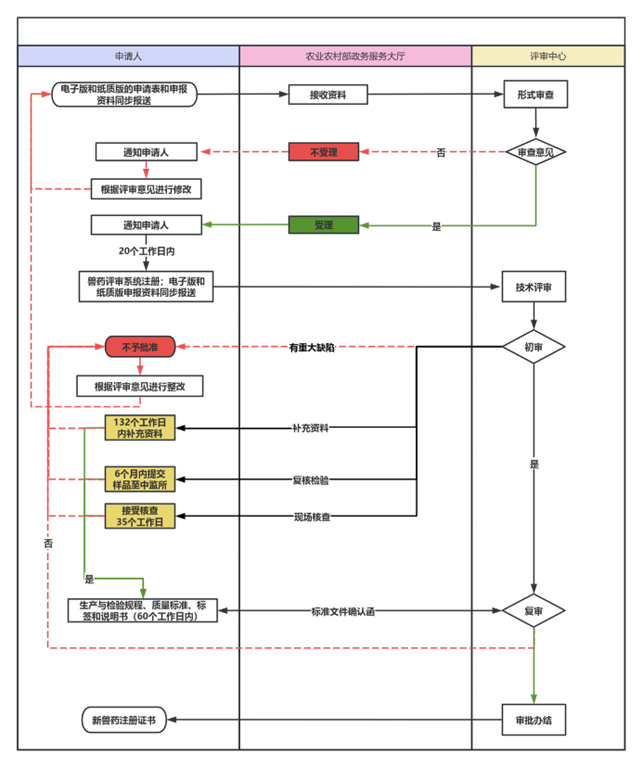
七、新兽药注册周期
ㅤㅤ资料齐全,注册周期1-2年;
ㅤㅤ资料不齐全,注册周期为3-5年,具体时间根据产品资料完整程度、试验周期以及评审进度而定。
八、我们的服务
ㅤㅤ1. 合规咨询与培训服务;
ㅤㅤ2. 检测实验室的质量审核与联系;
ㅤㅤ3. 检测报告质量审核服务;
ㅤㅤ4. 申报资料整理与编写服务;
ㅤㅤ5. 申报资料预审服务;
ㅤㅤ6. 注册资料递交与进度管理;
ㅤㅤ7. 注册预算与成本控制;
ㅤㅤ8. 兽药标签和说明书编写服务;
ㅤㅤ9. 年度报告编写和提交;
ㅤㅤ10. 进口兽药翻译服务。
联系方式
- 联系人:曹渭
- 电话:0757-28333064
- 邮箱:info@ehs.ac.cn
- 地址:广东省佛山市顺德区乐从镇佛山新城汾江南路235号依云国际财富中心2座103室
-
在线咨询
 点击图标
点击图标
专业客服 7x24H
为您服务 -
关注我们
 扫码关注公众号,获取更多企业信息
扫码关注公众号,获取更多企业信息
