
一、什么是兽药比对试验?
ㅤㅤ根据《兽药产品批准文号管理办法》第十五条,农业农村部在核发新兽药的兽药产品批准文号时,设立不超过5年的监测期。监测期满后,其他兽药生产企业可对列入兽药比对试验目录中的兽药产品进行仿制。通过申报兽药的受试品与已上市的参比品进行对比研究,以确保受试品与参比品在药学等效性、生物等效性以及临床效果等方面的一致性。
二、兽药比对试验目录
ㅤㅤ根据《兽药管理条例》和《兽药产品批准文号管理办法》,农业部制订了《兽药比对试验目录》以及相关要求,目前《兽药比对试验目录》已发布六批。

三、兽药比对试验的流程
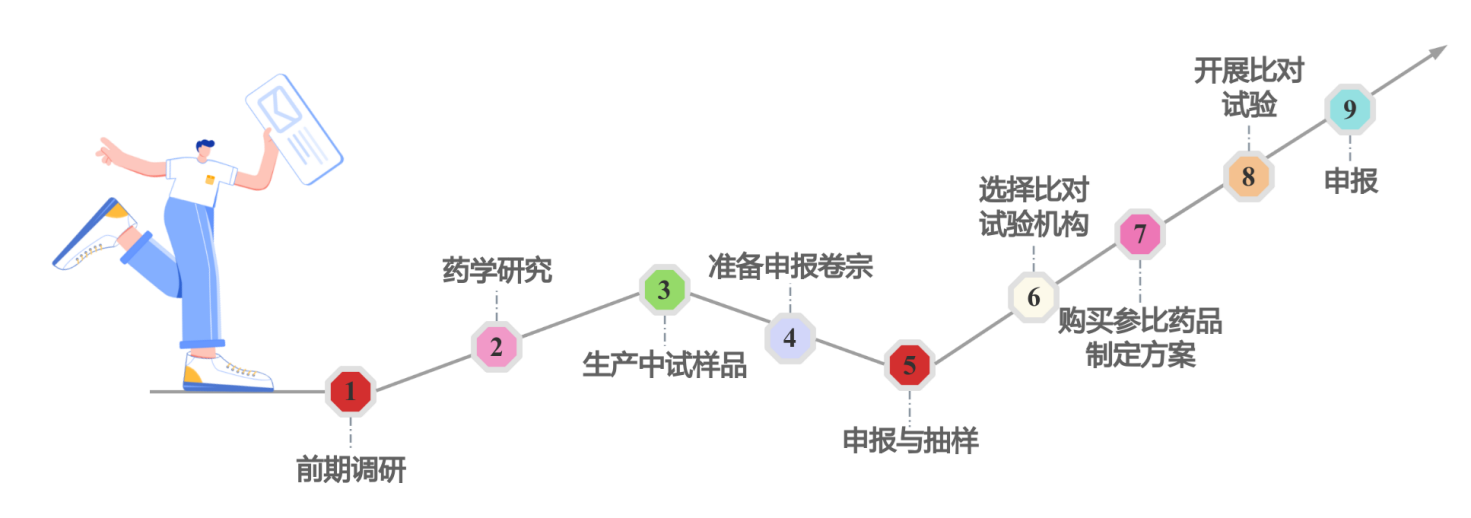
ㅤㅤ(1)前期调研
ㅤㅤ项目开展前需进行充分的调研工作,包括了解市场需求,评估仿制药的市场潜力和竞争情况、参比品是否被列入比对试验目录、仿制是否存在专利侵权的风险、参比品的购买途径、原材料的获得途径等。
ㅤㅤ(2)药学研究
ㅤㅤ调研确定好仿制的参比品后,企业可通过中国兽药信息网购买参比品,研究参比品的处方与生产工艺,按照兽药比对试验产品药学研究等资料要求(农办医[2016]60)完成药学研究。
ㅤㅤ(3)生产中试样品
ㅤㅤ处方和工艺确定后,需在GMP车间生产中试样品。进行比对试验的受试品应是符合企业标准对的兽药产品,并在兽药生产企业兽药GMP生产线上抽取。受试品经省级兽药检验机构按照企业标准复核检验合格后,方可用于比对试验
ㅤㅤ(4)准备申报卷宗
ㅤㅤ参照兽药产品批准文号管理办法(2022年1月7日农业农村部令2022年第1号修订)、兽药比对试验产品药学研究等资料要求(农办医[2016]60号)和兽药比对试验要求(农业农村部公告第787号)完成药学研究并整理好申报卷宗。
ㅤㅤ(5)申报与抽样
ㅤㅤ按照《兽药产品批准文号管理办法》的第十一条和第十二条,申请人应当向所在地省级人民政府兽医行政管理部门提交申请,由省级人民政府兽医行政管理部门进行现场核查、抽样和复核检验,共抽取三批样品,其中一批为在线抽样。
ㅤㅤ(6)选择比对试验机构
ㅤㅤ通过省级人民政府兽医行政管理部门初步审查的企业,将相关研究资料及加贴封签的在线抽样样品送至已获得相关试验资质的比对试验机构。
ㅤㅤ(7)购买参比药品、制定比对试验方案
ㅤㅤ企业可通过中国兽药信息网购买参比品,参比品原则上应是原研发生产企业的兽药产品,参比品的质量由申请比对试验的兽药生产企业负责,经生产企业检验或委托省级兽药检验机构、第三方检验机构合格后方可进行比对试验。
ㅤㅤ比对试验机构根据比对试验目录及指导原则要求制定比对试验方案。
ㅤㅤ(8)开展比对试验
ㅤㅤ比对试验机构应当严格按照要去比对试验指导原则开展比对试验,并完成试验报告,报告完成后将比对试验报告分送省级人民政府兽医行政管理部门和申请人。
ㅤㅤ(9)申报
ㅤㅤ全部试验完成后,省级人民政府兽医行政管理部门将现场核查报告、复核检验报告、比对试验方案、比对试验协议、比对试验报告、相关药学研究资料及全部申请资料一式一份报农业部;农业部送中监所组织专家评审,并作出决定是否核发兽药产品批准文号。
四、兽药比对试验中包含哪些试验?
ㅤㅤ按照《兽药产品批准文号管理办法》规定,申请兽药产品批准文号需要实施生物等效性试验和休药期验证试验。
ㅤㅤ生物等效性试验包括血药浓度法和临床疗效验证法。
五、哪些企业可以进行比对试验?
ㅤㅤ开展比对试验的检验机构应当遵守兽药非临床研究质量管理规范(GLP)和兽药临床试验质量管理规范(GCP),其名单由中国兽医药品监察所公布,同时比对试验开展机构与申请人不得是同一企业。目前符合兽药临床试验质量管理规范(GCP)的单位共80家,其中可提供比对试验研究的企业共22家。

六、如何购买比对试验中的参比品?
ㅤㅤ药学研究过程中的参比品由申请人自行购买,保留发票;比对试验中的参比品由比对试验单位从中监所购买。
七、环健安评可提供哪些服务?
ㅤㅤ(1)项目调研,提供调研报告;
ㅤㅤ(2)项目预算与成本控制;
ㅤㅤ(3)处方和工艺研究;
ㅤㅤ(4)原研药购买;
ㅤㅤ(5)委托测试;
ㅤㅤ(6)准备比对试验申报资料;
ㅤㅤ(7)资料递交与进度管理。
联系方式
- 联系人:曹渭
- 电话:0757-28333064
- 邮箱:info@ehs.ac.cn
- 地址:广东省佛山市顺德区乐从镇佛山新城汾江南路235号依云国际财富中心2座103室
-
在线咨询
 点击图标
点击图标
专业客服 7x24H
为您服务 -
关注我们
 扫码关注公众号,获取更多企业信息
扫码关注公众号,获取更多企业信息
