国产化妆品注册备案服务
一、相关法规依据
《化妆品监督管理条例》、《化妆品分类规则和分类目录》、《化妆品注册备案管理办法》、《化妆品注册备案资料管理规定》、《化妆品标签管理办法》、《化妆品功效宣称评价规范》、《化妆品安全评估技术导则(2021年版)》
二、法规概述
1. 化妆品的定义和分类
化妆品,是指以涂擦、喷洒或者其他类似方法,施用于皮肤、毛发、指甲、口唇等人体表面,以清洁、保护、美化、修饰为目的的日用化学工业产品。
化妆品分为特殊化妆品和普通化妆品。用于染发、烫发、祛斑美白、防晒、防脱发的化妆品以及宣称新功效的化妆品为特殊化妆品。特殊化妆品以外的化妆品为普通化妆品。
2. 化妆品的监管
国家按照风险程度对化妆品实行分类管理。国家对特殊化妆品实行注册管理,对普通化妆品实行备案管理。
国家药品监督管理局负责特殊化妆品、进口普通化妆品的注册和备案管理,并指导监督省、自治区、直辖市药品监督管理部门承担的化妆品备案相关工作。国家药品监督管理局可以委托具备相应能力的省、自治区、直辖市药品监督管理部门实施进口普通化妆品备案管理工作。
特殊化妆品经国务院药品监督管理部门注册后方可生产、进口。国产普通化妆品应当在上市销售前向备案人所在地省、自治区、直辖市人民政府药品监督管理部门备案。
国务院药品监督管理部门依照本条例第十三条第一款规定的化妆品新原料注册审查程序对特殊化妆品注册申请进行审查。对符合要求的,准予注册并发给特殊化妆品注册证;普通化妆品备案人通过国务院药品监督管理部门在线政务服务平台提交本条例规定的备案资料后即完成备案。
3. 化妆品注册申请人、备案人应当具备下列条件:
(1)是依法设立的企业或者其他组织;
(2)有与申请注册、进行备案的产品相适应的质量管理体系;
(3)有化妆品不良反应监测与评价能力。
特殊化妆品注册证有效期为5年。有效期届满需要延续注册的,应当在有效期届满30个工作日前提出延续注册的申请。
三、国产化妆品注册备案资料
1. 《化妆品注册备案信息表》及相关资料;
2. 产品名称信息;
3. 产品配方(包括原料序号、原料名称、百分含量、使用目的、原料安全信息);
4. 产品执行的标准;
5. 产品标签样稿;
6. 产品检验报告(包括微生物和理化检验、毒理学试验、人体安全性试验和人体功效试验报告等);
7. 产品安全评估资料;
具体要求详见《国家药监局关于发布<化妆品注册备案资料管理规定>的公告》(2021年第32号)第三章。
四、国产化妆品注册备案流程
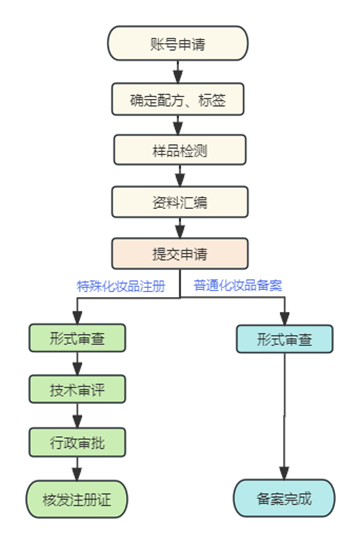
五、环健安评的服务
1. 产品注册备案全过程的代理服务;
2. 辅助开通账户;
3. 辅助企业完成注册前授权和公证事项;
4. 辅助注册备案资料的编写;
5. 注册备案资料预审服务及申报过程中技术指导服务;
6. 注册备案配方和原文标签的合规审核;
7. 中文标签的合规审核;
8. 产品安全和功效检测监理服务;
9. 产品安全评估资料编写审核技术服务。
六、环健安评的优势
1. 专业法规团队:拥有专业的技术服务团队,一对一定制化技术服务。
2. 资源优势:拥有高质量合作伙伴,帮助客户选择试验机构、高效对接试验。
3. 完善的服务体系: 从咨询、检测、注册备案到培训,提供全方位的服务。
4. 合理的费用预算:通过提高团队效率,为客户提供优惠的价格和优质的专业服务。

常见问题
浏览更多质量安全负责人能否在不同的化妆品注册人、备案人、受托生产企业兼任?
为保障化妆品质量安全,确保质量安全负责人依法落实产品质量安全管理和产品放行职责,按照“一证一人”的原则,申请两个以上(含两个)的化妆品生产许可,不得由同一个自然人担任上述企业的质量安全负责人;不同的化妆品注册人、备案人,不得由同一个自然人担任质量安全负责人。化妆品注册人、备案人与受托生产企业属于同一集团公司,执行同一质量管理体系,受托生产企业接受该注册人、备案人的委托生产化妆品时,该注册人、备案人与受托生产企业可以聘用同一个自然人担任质量安全负责人。
染发产品含有Ⅰ剂、Ⅱ剂,有两个配方,如何申请注册?
根据《化妆品注册备案资料管理规定》第三十五条,包含两个或者两个以上必须配合使用或者包装容器不可拆分的独立配方的化妆品,应当分别填写配方,按一个产品申请注册。染发产品的两剂为必须配合的产品,需要分别填写配方,按一个产品申请注册。
产品备案资料提交后在未公示之前是否可以进行变更操作?
产品备案资料提交完成需在监管端完成“资料整理”环节之后才可以进行变更操作。
同一种原料生产商应该填报一家还是可以多家?
同一种原料的生产商需根据该原料质量规格填报,多家生产商的原料质量规格一致,可填报多家,如果不一致,则需分别填报。
通用名使用具体原料名称或者表明原料类别的词汇的,该原料的使用目的应如何填报?
根据《化妆品标签管理办法》第八条,通用名使用具体原料名称或者表明原料类别的词汇的,应当与产品配方成分相符,且该原料在产品中产生的功效作用应当与产品功效宣称相符。因此,该原料在配方中的使用目的应当与产品功效宣称相符。使用动物、植物或者矿物等名称描述产品的香型、颜色或者形状的除外。
特殊化妆品不予注册, 再次申报资料的要求是什么,可以使用复印件吗?
根据《化妆品注册备案资料管理规定》第五十八条,对于非安全性原因不予注册的特殊产品再次申请注册时,可使用原注册资料的复印件,同时提交不予注册未涉及安全性的说明,包括对不予注册原因的解释。
普通化妆品备案是否存在有效期?
原国家食品药品监督管理总局《关于调整化妆品注册备案管理有关事宜的通告》(2013年第10号)规定,应当自备案之日起,每满4年重新确认产品备案信息,不再生产的,企业应当主动注销原备案信息。 2021年《化妆品注册备案管理办法》实施后,普通化妆品不再存在有效期的概念而换成年度报告制度。根据国家药监局《关于实施<化妆品注册备案资料管理规定>有关事项的公告》(2021年第35号),自2022年1月1日起,通过原注册备案平台和新注册备案平台备案的普通化妆品,统一实施年度报告制度。备案人应当于每年1月1日至3月31日期间,通过新注册备案平台,提交备案时间满一年普通化妆品的年度报告。
普通化妆品哪些情形需要加测人体安全性试用试验?
(1)驻留类产品理化检验结果pH≤3.5或企业标准中设定pH≤3.5的产品应当进行人体试用试验安全性评价。 (2)宣称祛痘、抗皱、祛斑等功效的淋洗类产品均应当进行人体试用试验安全性评价。 两剂或两剂以上混合使用的产品,应按说明书中使用方法进行试验。当存在不同浓度、不同配比等与安全性相关的不同使用方法时,需对每一种情况均进行相关的人体安全性检验。
在不豁免毒理学试验时,哪些产品应开展急性眼刺激试验?
根据《化妆品注册和备案检验工作规范》(2019年第72号公告),易触及眼睛的产品须进行急性眼刺激性试验。常见易触及眼睛的产品包括洗面奶、洗发水、冲洗型护发素、眼部产品(描眉类彩妆除外)、沐浴露等。
联系方式
- 联系人:曹渭
- 电话:0757-28333064
- 邮箱:info@ehs.ac.cn
- 地址:广东省佛山市顺德区乐从镇佛山新城汾江南路235号依云国际财富中心2座103室



