
一、什么是注册检验?
ㅤㅤ兽药注册检验是指对申请注册的新兽药进行的一系列检验和评估,以确保其质量、安全性和有效性符合国家标准。注册检验包括样品检验和兽药质量标准复核两个方面。这是新兽药注册过程中的一个重要环节。新兽药通过初审,认为建立的质量控制方法可行,方法学验证资料完整可靠后,申请人应向中国兽医药品监察所提供兽药注册检验所需要的有关资料和样品进行注册检验。
二、注册检验的受理范围?
ㅤㅤ农业农村部下达的新兽药和进口兽药注册检测。
三、注册检验样品、试剂和耗材要求
ㅤㅤ(1)样品要求
ㅤㅤ申请人应提供连续3个批次的样品(化学药品每个规格提供3批),每批样品数量应至少为全部检验项目检验用量的3倍。
ㅤㅤ样品剩余效期应不少于6个月。
ㅤㅤ样品应包装完整并贴有标签,标签应根据报送兽药评审中心的兽药标签设计样稿(终稿)进行印制。
ㅤㅤ(2)检验所需相关试剂、耗材要求
ㅤㅤ兽用生物制品注册检验需提供检验所需专用试剂(或配制SOP)、菌(毒、虫)种、细胞、标准物质及其他所需生物活性材料和特殊实验耗材等,以上材料均需满足样品检验2次用量。
ㅤㅤ化学药品注册检验中需要使用标准物质的,一般应至少提供3支,且满足全部检验用量的3—5倍。除此之外,还应提供非常用试剂和耗材,包括一般国内无法购买的试剂、购买存在困难的试剂、易制毒试剂等;指定品牌或规格的检验用色谱柱;兽药残留检测方法复核相关耗材;其他检验用特殊设施、设备或材料等。
ㅤㅤ化药新标准物质原料应按兽用化药标准物质原料受理程序和要求,提供制备相关兽药标准物质的原料和标定用标准物质。
四、注册检验用资料
| 兽用生物制品 | |||
| 文件名 | 属性 | 数量 | 备注 |
| 申请人自检报告 | 原件 | 1份 | / |
| 批生产和检验记录 | 复印件 | 1份 | 批生产和检验记录需装订成册,并在书脊上标明申请人名称和样品名称。 |
| 试剂清单 | / | 1份 | 应标明名称、规格、批号、数量、保存条件、生物学参数、有效期至等。 |
| 菌(毒、虫)种、细胞、标准物质以及生物活性材料应提供检定报告。 | / | 1份 | / |
| 涉及菌(毒、虫)种的需提供承诺书。 | / | 1份 | / |
| 检验相关SOP、说明书和内标签设计样稿。 | / | 1份 | 上述材料不需装订,页底须标明页码,其中SOP、说明书和内标签设计样稿 必须与报送兽药评审中心申报资料最终稿保持一致。 |
| 兽用化学药品 | |||
| 文件名 | 属性 | 数量 | 备注 |
| 申请人自检报告 | 原件 | 1份 | / |
| 质量标准起草说明与质量标准方法学研究资料。 | / | 1份 | 装订成一册,在封面须标明申报单位名称和样品名称,应有内容目录并标明页码。 |
| 非国家法定标准物质的检定报告、标定研究资料和承诺书。 | / | 1份 | 应标明名称、规格、批号、数量、保存条件、生物学参数、有效期至等。 |
ㅤㅤ新标准物质原料应按兽用化药标准物质原料受理程序和要求,报送有关研究资料并填写兽药标准物质原料受理单。
ㅤㅤ进行兽药残留检测方法复核的应提供方法研究资料及验证报告。
五、注册检验的流程
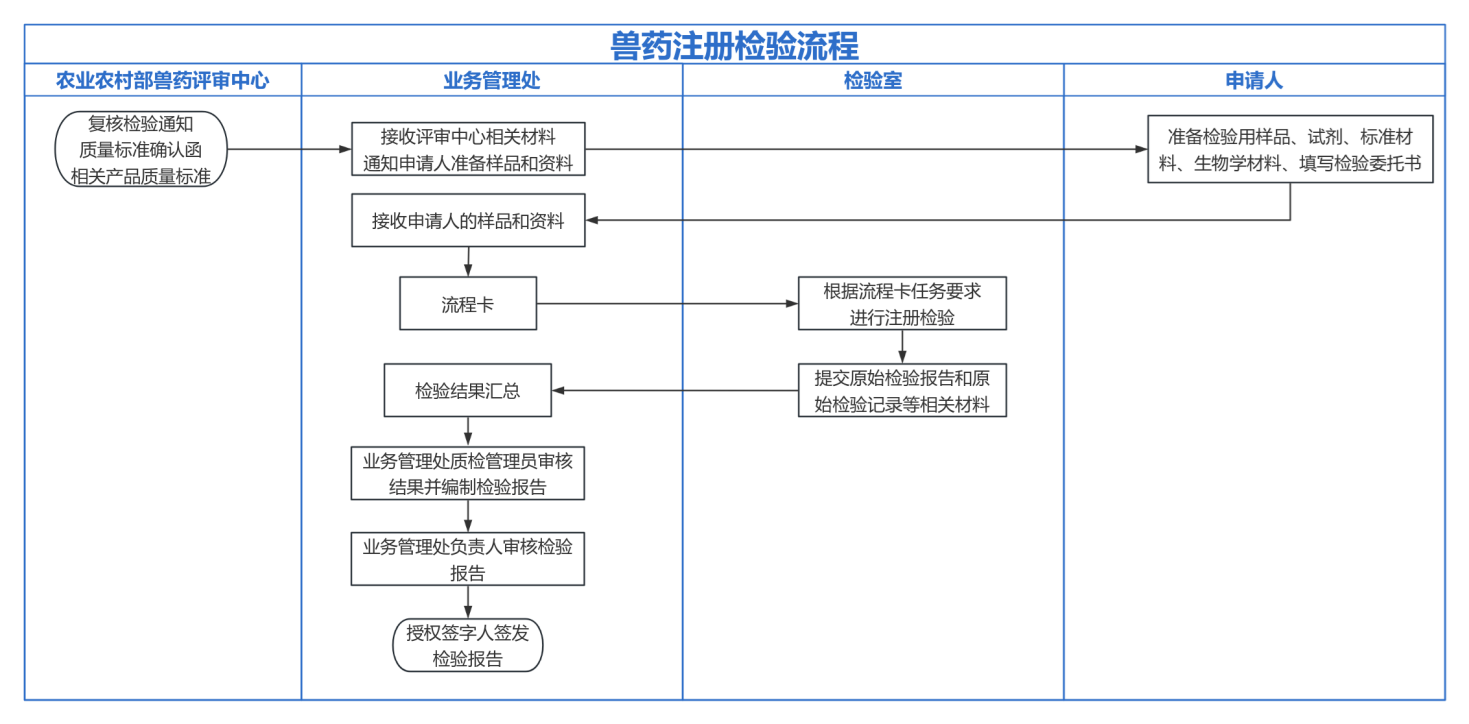
六、注册检验时限
ㅤㅤ接到复核检验通知和样品后,在90个工作日内完成样品检验,出具检验报告书;需用特殊方法检验的在120个工作日内完成。
ㅤㅤ要进行样品检验和兽药质量标准复核的,在120个工作日内完成;需用特殊方法检验的兽药在150个工作日内完成。
ㅤㅤ计时起点为签订《检验委托书》的日期,终点为签发检验报告的日期。因品种特殊及检验工作中的特殊情况,需要延长检验时限的,由中国兽医药品监察所向农业农村部法规司提出暂停计时申请。
七、注意事项
ㅤㅤ由于申请人提交的质量标准、残留检测方法以及标准物质,菌(毒、虫)种等出现问题而导致检验无法进行的,按一次检验不合格计。
ㅤㅤ检验过程中不允许申请人与检验室及检验员私自沟通,检验问题和咨询事宜由业务管理处负责统一沟通协调。
ㅤㅤ凡生物活性材料涉及高致病性动物病原微生物的,应按相关法律法规要求运输,确保生物安全。
ㅤㅤ申请人务必于送样前5个工作日与中国兽医药品监察所业务管理处联系。
八、环健安评可提供哪些服务
ㅤㅤ(1)法规咨询;
ㅤㅤ(2)准备注册检验相关样品和资料;
ㅤㅤ(3)注册检验资料递交与进度管理;
ㅤㅤ(4)实验数据及资料缺口分析。
联系方式
- 联系人:曹渭
- 电话:0757-28333064
- 邮箱:info@ehs.ac.cn
- 地址:广东省佛山市顺德区乐从镇佛山新城汾江南路235号依云国际财富中心2座103室
-
在线咨询
 点击图标
点击图标
专业客服 7x24H
为您服务 -
关注我们
 扫码关注公众号,获取更多企业信息
扫码关注公众号,获取更多企业信息
